数字化转型网企业出海将关注品牌出海,全球化战略,合规与风控,供应链管理,数据保护与隐私安全,知识产权,税务,海外团队建设,海外运营,人力资源管理,组织管理等企业出海、全球化相关全产业链相关环节。点击图片或扫描图片二维码,加入数字化转型网企业出海研习社:

近年来,在国家政策导向的指引下,越来越多的中国医疗器械企业加快“走出去”的步伐,医疗器械企业出海成为发展热潮。根据海关总署的数据,2020年中国医疗器械出口额达到181亿美元以上,同比增长40%以上。2023年中国医疗仪器及器械出口金额达到184.18亿美元。据统计,2022年中国器械生产商在美国海外注册中占比高达27.84%。[1]然而,在出海的过程中企业亦往往面临着复杂的法律和监管问题。本文拟分享一些医疗器械企业常见的出海方式及案例,并就医疗器械企业出海在境内及目的地国家的法律监管要点进行探讨,以供医疗器械出海企业参考。
一、医疗器械企业出海常见方式及案例
医疗器械企业常见出海模式可分为加入海外供应链、订单出海、自主出海三种类型。其中,加入海外供应链模式是指企业承担产品设计、制造等环节,形成“代工”的OEM或者“贴牌”的ODM类型的出海;订单出海模式是指主要依赖海外经销商,订单和品牌建设处于初期环节,基本没有售后服务;自主出海模式是指建立本土化销售团队、构建产品分装和物流中心、搭建售后服务团队,大规模扩大海外销售。[2]以下就各出海模式列举一些医疗器械企业案例供参考。
1. 加入海外供应链
(1)青岛海泰新光科技股份有限公司(“海泰新光”)
海泰新光主要从事医用内窥镜器械和光学产品的研发、制造、销售和服务。公司目前主要采用直销的销售模式,包括ODM、OEM和自主品牌三种业务类型,2023年度业务占比分别为65.89%、20.41%和13.70%。公司在美国设有OMEC Medical Inc.和OMEC Medical (NV) Inc.两家海外公司,分别负责内窥镜的维修和焊接封装业务、封装业务和一次性内窥镜研发与生产。[3]通过增资全资孙公司OMEC Medical (NV) Inc.实施募投项目,海泰新光将进一步扩大在海外市场的业务布局。[4]公司在2024年将持续深化ODM业务,同时加大自主品牌产品的市场推广和销售力度。为了进一步推进两部分业务进程,2024年将重点实施完成美国子公司和泰国子公司生产线建设,实现内窥镜海外生产。[5]根据海泰新光2024年相关研究报告[6]和公司公告,其股权架构如下图所示:数字化转型网www.szhzxw.cn
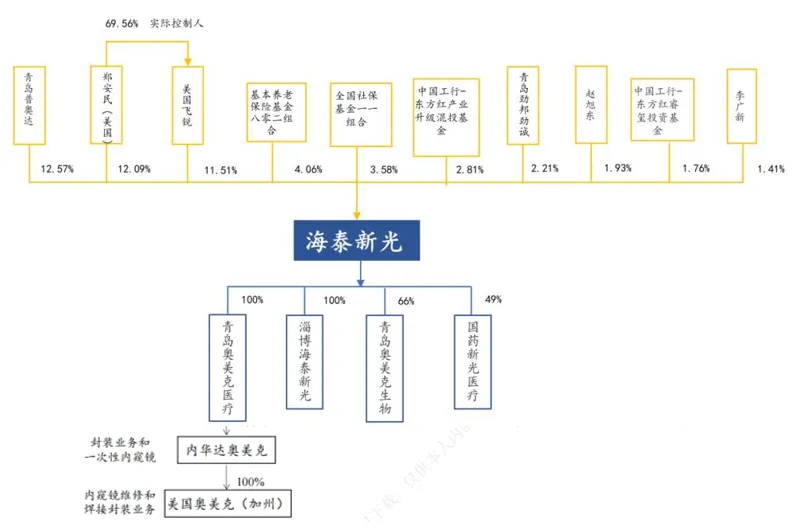
(2) 采纳科技股份有限公司(“采纳股份”)
采纳股份主要从事注射穿刺器械及实验室耗材的研发、生产和销售,公司通过ODM/OEM等方式为许多全球知名医疗企业提供穿刺针、注射器、实验室耗材等相关产品。从产品类型上看,公司ODM模式下覆盖了注射穿刺类器械的所有主要产品,OEM模式主要以试剂管、过滤盒以及部分兽用穿刺针产品为主。公司境外市场主要包括美国、欧洲及英国等国家和地区,客户多为全球知名医用及动物用产品企业,合作关系稳定。采纳股份于2023年2月在美国特拉华州设立了子公司Wttod US INC.(卫图德美国有限公司),持股比例100%。截至目前,采纳股份尚未实缴出资,该境外子公司尚无实际经营业务。[7]根据采纳股份2023年年度报告“三、股东和实际控制人情况”,其股权架构如下图所示:
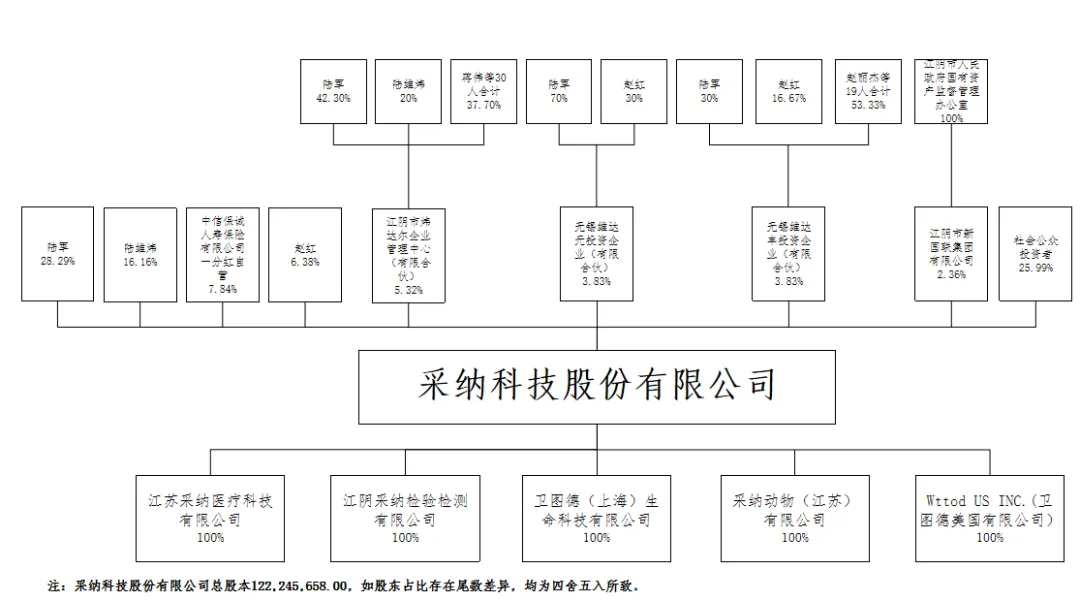

2. 订单出海
(1) 浙江拱东医疗器械股份有限公司(“拱东医疗”)
拱东医疗是一家专业从事一次性医用耗材的研发、生产及销售的高新技术企业。公司采用以客户需求为导向的“以销定产”生产模式。对于境外市场需求,公司采用按订单生产的模式,外销业务员接到订单后交由计划物控部门组织订单评审,评审通过后确定物料需求并安排生产计划,在约定期限内完成生产并发货。为开拓和维护美国市场,拱东医疗于2014年设立了美国全资子公司GD Medical。2023年1月,公司以自有资金4,500万美元对GD Medical进行增资,通过业务合并的方式吸收合并原TPI业务及资产,这有利于公司进一步拓展在美国市场的相关业务,为美国客户提供本土化服务;同时,发挥中美经营主体的各自优势、资源互补的协同作用,为公司获取新客户、新市场、新技术提供了良好的平台。[8]根据《浙江拱东医疗器械股份有限公司首次公开发行股票招股说明书》“五、发行人股权结构及组织结构”,其股权架构如下图所示。结合公司2024年半年度报告,2023年2月,原公司美国子公司GD Medical, Inc.更名为Trademark Plastics Inc.,公司的海外架构仍维持对Trademark Plastics Inc.的100%全资持股。
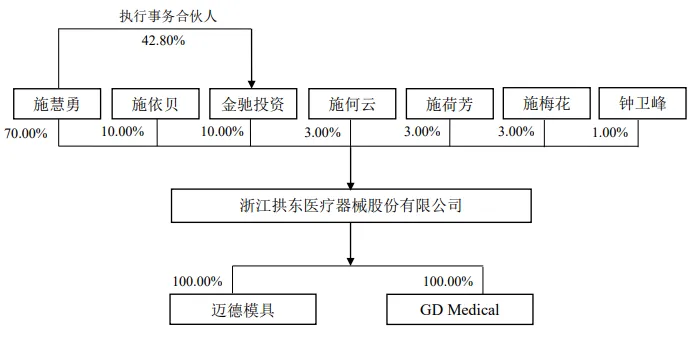
(2) 广州洁特生物过滤股份有限公司(“洁特生物”)
洁特生物是主要从事细胞培养类及与之相关的液体处理类生命科学耗材研发、生产和销售的高新技术企业。在销售渠道方面,公司深耕生命科学耗材市场多年,在国内外均已形成覆盖面较广的销售网络渠道。公司产品对外出口至美国、德国、英国、澳大利亚、印度、巴西和阿根廷等几十个国家和地区,拥有一批长期友好合作的国外ODM客户和经销商。外销业务方面,公司采取“以销定产”的方式组织生产,一般不进行产成品备货,而是根据订单情况下达生产任务,实行按单生产、按需生产的模式。2023年7月,公司新设立美国全资子公司JET LIFE SCIENCES CO. INC.,该公司将主要开展自有品牌产品在美国的销售,目前尚在前期筹备阶段。[9]根据洁特生物公司相关公告(截至2024年8月),其股权架构如下图所示:
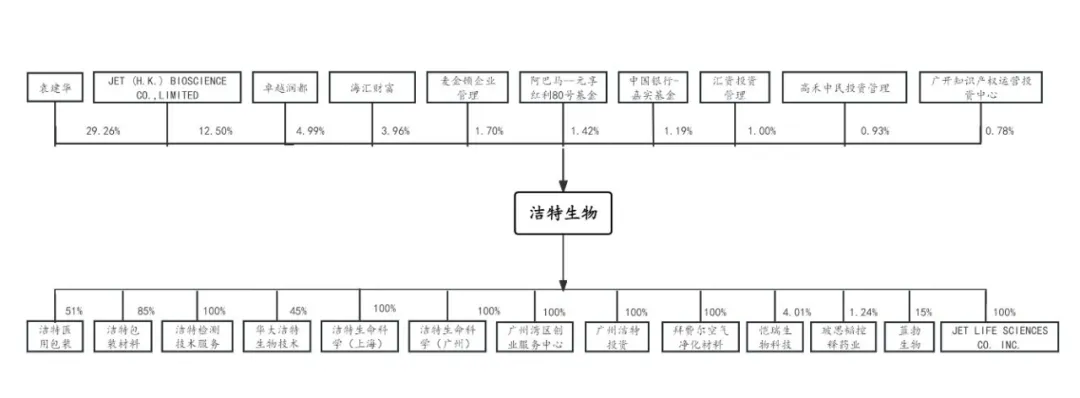
3. 自主出海
(1) 深圳迈瑞生物医疗电子股份有限公司(“迈瑞医疗”)
迈瑞医疗主要从事医疗器械的研发、制造、营销及服务,主要产品覆盖三大领域:生命信息与支持、体外诊断以及医学影像。历经多年的发展,迈瑞医疗已经成为全球领先的医疗器械以及解决方案供应商,在北美、欧洲、亚洲、非洲、拉美等地区的约40个国家设有境外子公司,产品远销190多个国家及地区。目前,公司已建立起基于全球资源配置的研发创新平台,在美国硅谷、美国新泽西、美国明尼苏达、芬兰海肽和德国德赛均设有研发中心,形成了庞大的全球化研发、营销及服务网络。与此同时,公司已在中国40多家分公司、50余家驻地服务站,以及海外40多个国家和地区部署了直属服务团队。在全球范围内,公司培养和发展了2,000多家服务渠道商,遍及全球190多个国家和地区,并配备超过10,000名拥有服务资质的渠道商服务人员为客户提供服务。同时,公司在海外部署了多个直属备件仓库和培训中心。[10]根据《深圳迈瑞生物医疗电子股份有限公司首次公开发行股票并在创业板上市招股说明书(申报稿)》“五、发行人股权结构和组织结构”,其股权架构如下图所示。结合2024年公司半年度报告,迈瑞医疗目前在境外设有63家境外子公司;在国内设有35家子公司、30余家分支机构。
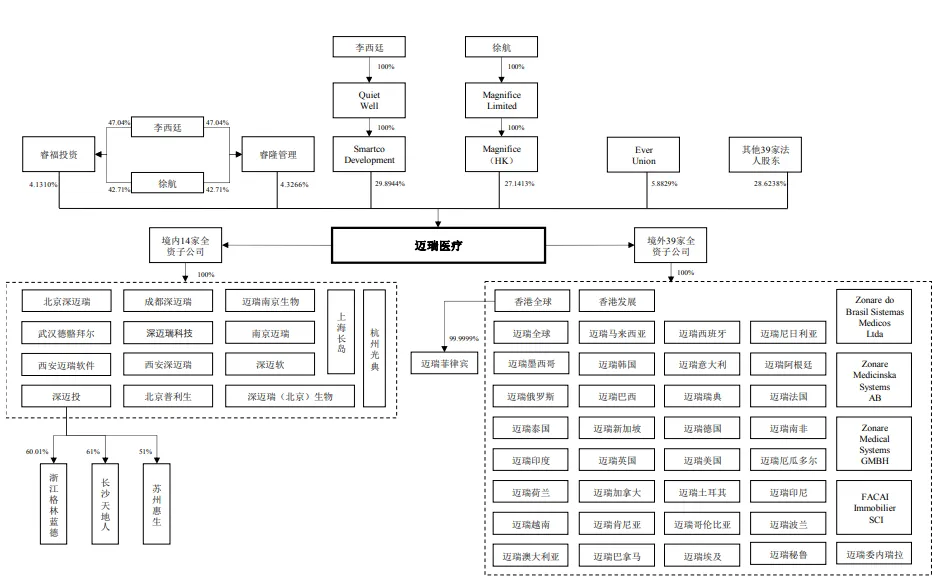

(2)上海联影医疗科技股份有限公司(“联影医疗”)
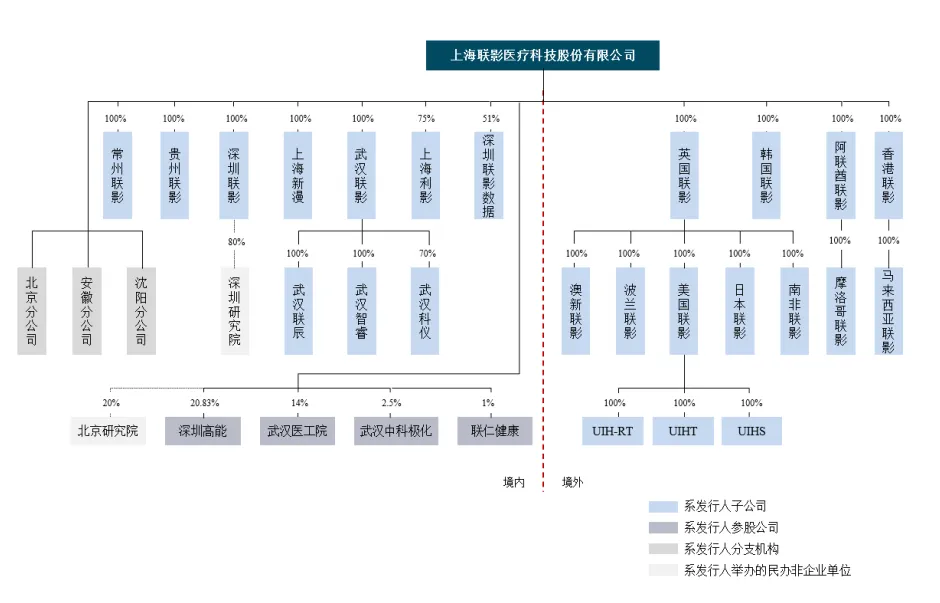
联影医疗致力于为全球客户提供高性能医学影像设备、放射治疗产品、生命科学仪器及医疗数字化、智能化解决方案。[11]公司专注于“一核多翼,高举高打,全线突破”的市场战略,从海外产品注册、团队和网络建设、生产基地和供应链布局等多方面入手,积极推进海外业务发展。目前,公司业务已覆盖亚洲、美洲、欧洲、大洋洲、非洲等全球70多个国家和地区。[12]在生产模式方面,公司采取自主生产模式,在上海、常州、武汉、美国休斯敦等进行产能布局。联影医疗生产全线产品,UIHT负责公司部分整机产品的生产。在全球营销体系建设方面,截至2023年,公司在全球建立了超30个区域总部、销售平台和分/子公司。在全球服务网络建设方面,公司全球服务网络建设覆盖达到60余个国家/地区,全面海外服务次数(不含工作站)超5,000次,客户服务点遍布全球各地,全球服务团队已超1,000人,分布于多个国家和地区。[13]根据《上海联影医疗科技股份有限公司首次公开发行股票并在科创板上市招股说明书》“五、公司的股权结构图”,其股权架构如下图所示。结合联影医疗2024年半年度报告,公司的海外架构目前拥有19家境外子公司。数字化转型网www.szhzxw.cn
二、出海架构搭建境内的法律监管要点
1. ODI审批问题
如果医疗器械企业通过出境收购或者设立新公司的方式搭建海外架构,根据《企业境外投资管理办法》(国家发展和改革委员会令第11号)、《境外投资管理办法》(商务部令2014年第3号)、《国家外汇管理局关于进一步简化和改进直接投资外汇管理政策的通知》(汇发[2015]13号)等有关规定,中华人民共和国境内企业直接或通过其控制的境外企业,以投入资产、权益或提供融资、担保等方式,获得境外所有权、控制权、经营管理权及其他相关权益的投资活动,需要进行境外投资审批(“ODI审批”)。ODI审批的流程涉及发改委备案/核准、商务部门备案/核准及外汇登记。
在实务中,原则上ODI审批无实质障碍,但由于各个地区政策和实操流程原因,在审批的难易程度和时间上存在一定差异。另外,近些年监管部门在加强对外投资一些领域的限制。根据国务院《关于进一步引导和规范境外投资方向指导意见的通知》(“《意见》”),明确将境外投资项目分成了鼓励开展、限制开展和禁止开展三类情形,《意见》限制开展的境外投资包括房地产、酒店、影城、娱乐业、体育俱乐部等境外投资及不符合投资目的国环保、能耗、安全标准的境外投资等。
如果未办理ODI登记,实践中可能导致公司无法汇出后续投资款项、无法办理境外投资企业利润汇回等资本项下的外汇业务,且面临行政处罚的风险。实践中存在不少未办理ODI登记被处罚的公开案例。
2. 37号文登记问题
如果医疗器械企业通过红筹方式[14]搭建海外架构,则根据《国家外汇管理局关于境内居民通过特殊目的公司境外投融资及返程投资外汇管理有关问题的通知》(汇发[2014]37号)(“37号文”)的规定,创始人需要进行37号文登记。未进行37号文登记,不仅创始人面临相关处罚风险、公司外汇业务可能受控,未来也会影响公司资金的跨境流动。数字化转型网www.szhzxw.cn
在深外管检[2023]40号案例中,2023年11月27日,林某因设立海外特殊目的公司未办理37号文外汇登记,同时发生资金流出,违反了37号文第十五条规定,具体表现为“通过虚假或构造交易汇出资金用于特殊目的公司”或“在资金流出前未按规定办理相关外汇登记”。鉴于林某的行为已构成逃汇事实,外汇管理部门依据《中华人民共和国外汇管理条例》第三十九条的规定,按照逃汇金额的一定比例对林某进行了处罚,最终林某被处以人民币185.9万元的罚款。

3. 境内数据出境合规问题
境内现行数据出境合规监管的法律法规主要包括《网络安全法》《数据安全法》《个人信息保护法》《数据出境安全评估办法》《个人信息出境标准合同办法》《促进和规范数据跨境流动规定》等。
根据现行数据合规相关规定,数据出境的合规方式主要有三种:数据出境安全评估、订立个人信息出境标准合同及备案、通过个人信息保护认证,相关法规对其适用的情形进行了区分。另外,根据《促进和规范数据跨境流动规定》,自贸区在国家数据分类分级保护制度框架下,可以自行制定区内需要纳入数据出境安全评估、个人信息出境标准合同、个人信息保护认证管理范围的数据清单。目前,中国(天津)自由贸易试验区、中国(北京)自由贸易区、中国(上海)自由贸易试验区临港新片区等已经发布各自的数据出境负面清单或一般数据清单。
另外,特殊行业数据出境(如人类遗传资源)受到特殊限制。如,根据《中华人民共和国人类遗传资源管理条例(2024修订)》的规定,人类遗传资源信息出境应当向国务院卫生健康主管部门备案并提交信息备份,可能影响我国公众健康、国家安全和社会公共利益的,还应当通过国务院卫生健康主管部门组织的安全审查。数字化转型网www.szhzxw.cn
4. 境内其他合规问题
医疗器械企业出海(尤其是通过订单出海)还可能涉及境内资质要求、合同履行等相关问题。在境内的资质要求方面,根据相关法律法规,从事货物进出口或者技术进出口的对外贸易经营者,应当向国务院对外贸易主管部门或者其委托的机构办理备案登记,只有拥有进出口权的企业,才可依法自主地从事进出口业务。另外,根据《医疗器械生产监督管理办法》、《医疗器械经营监督管理办法》及《医疗器械产品出口销售证明管理规定》,医疗器械企业出口,如果经营的是二类医疗器械,需要办理医疗器械经营备案;经营的是三类医疗器械,需要办理医疗器械经营许可。我国已取得医疗器械产品注册证书及生产许可证书,或已办理医疗器械产品备案及生产备案的,食品药品监督管理部门可为相关生产企业出具《医疗器械产品出口销售证明》。
此外,企业还面临着合同履行的风险,包括经销商资质、产品标准、产品使用说明、货款支付、适用法律等。例如,在经销商资质方面,如买家为外国经销商,出口企业需核查其所在的国家和地区是否要求医疗器械的经销商具备经销资质。在产品使用说明方面,合同中需要对医疗用品的适用范围、正确的使用规范进行详细说明,或在产品外包装上书写清晰、详尽,避免使用不当致使产品使用效果减弱或达不到规定标准。数字化转型网www.szhzxw.cn
实践中,企业上市时,监管部门也会关注出海企业向境外销售的合规问题,如康华生物(300841.SZ)曾被反馈要求“补充说明发行人向境外销售疫苗产品是否履行相应的审批程序”;奥美医疗(002950.SZ)曾被反馈要求说明“生产经营与海外销售产品是否满足境内相关产品监管、注册等监管要求”。
三、出海目的地国家的法律监管要点
1. 外资准入限制及审批
中国企业出海投资应首先考虑目的地国家的外商准入限制,如许多国家在某些产业如高科技、互联网、通信、金融、基础设施等对外资采取市场准入限制或禁止外资进入,中国企业想要通过投资拓展海外业务的将受制于相应的准入规则。如在美国,美国外国投资委员会(“CFIUS”)会对外国在美国的直接或间接投资进行监管,审查该等投资是否会对美国的国家安全造成威胁。美国的CFIUS制度的强制申报要求针对的是从事TID业务(TID U.S. business),即涉及关键技术、关键基础设施、敏感个人数据的美国企业。[15]当涉及外国政府拥有实质性利益的外国个人或实体收购TID美国企业的实质性股权,或涉及生产、设计、测试、制造、加工或开发需美国出口许可的关键技术的TID美国企业的特定交易,将触发强制性申报义务。

对于医疗器械而言,美国《2018年出口管制改革法案》(Export Control Reform Act of 2018, “ECRA”)相关法规出台后,被归类为“新兴和基础技术”的特定技术则会自动成为CFIUS出台的《2018年外国投资风险评估现代化法案》(Foreign Investment Risk Review Modernization Act of 2018, “FIRRMA”)中定义的“关键技术”。依据ECRA,生物技术、脑机接口、先进材料等14项技术类别被列入了“新兴和基础技术”的拟定清单。医疗器械出海企业如果涉及投资或者收购美国的上述涉及“新兴和基础技术”的企业,或在将来可能触发CFIUS申报义务。
实践中,CFIUS就曾迫使Patients Like Me剥离深圳市碳云智能科技有限公司(“碳云智能”)的投资。2017年,美国在线患者社区门户网站Patients Like Me 募集了1亿美元投资,并把多数股权出售给了中国投资者碳云智能。2018年8月,特朗普签署FIRRMA,该法案扩大了CFIUS对27个行业的审查权限,范围包括生物科技研发。2018年底,CFIUS以“收录美国患者数据会危及美国国家安全”为由,通知Patient Like Me 剥离其来自碳云智能的1亿美元投资及该公司股权。2019年4月,CFIUS迫使碳云智能出售其持有的Patients Like Me股权。2019年6月,碳云智能遵守CFIUS的命令,将Patients Like Me出售给美国公司United Health Group Inc。[16]数字化转型网www.szhzxw.cn
2. 出口管制
根据美国出口管制法规,美国原产技术,以及使用美国特定原产技术、软件生产的直接产品(不论其生产地区)等将均有可能受到美国出口管制规则的管辖并受限于商务部工业与安全局(“BIS”)对其进出口及销售业务的许可审查要求。尤其在半导体、人工智能、先进材料、先进计算、超算等关键技术领域,相关管制要求更加容易触发。在医疗器械领域,ECRA要求美国政府列入对国家安全有重要影响的“新兴和基础技术”。为回应ECRA关于指定新兴与基础技术的要求,2018年BIS发布了包括生物技术、脑机接口、先进材料等14项技术类别的拟定清单,该清单初步划定了新兴技术的范围。
2020年12月18日,BIS将医疗器械行业公司“中国科学器材有限公司”(CNSIM或CSIMC)列入实体清单,BIS以中国科学器材有限公司在中国滥用基因收集、分析或高技术监控,参与大规模侵犯人权的活动,和/或为中国出口协助世界各地专制政权的物品提供便利,违背美国外交政策利益为由将其列入清单。并采取对用以检测、识别和治疗传染病所必需的项目实施逐案审查的许可证审查政策,而对所有其他出口受《出口管理条例》(Export Administration Regulations, “EAR”)限制的项目实施推定许可拒绝的政策对该公司施加限制。数字化转型网www.szhzxw.cn
因此,医疗器械企业在出海布局的情况下,将美国技术以及相关衍生产品对境内公司进行输入及其后续转售时,都需谨慎评估可能存在的出口管制风险敞口并严格执行合规措施,否则将可面临被美国政府列入实体清单等严控名单,被处以刑事、行政处罚及承担高额罚金等不利后果。
3. 数据合规
医疗器械企业出海在境外运营过程中,可能涉及收集境外用户的个人数据和隐私信息,而该等数据的收集和使用会受到境外目的地国家数据安全合规的监管。如,2024年2月28日,拜登总统签发了一项行政命令《关于防止受关注国家获取美国人士大量敏感个人数据和美国政府相关数据的行政命令》(Executive Order on Preventing Access to Americans’ Bulk Sensitive Personal Data and United States Government-Related Data by Countries of Concern, “《行政命令》”),美国司法部于同日配套发布了关于该《行政命令》拟议规则制定的预先通知(Advance Notice of Proposed Rulemaking, ANPRM)的事实说明(“《事实说明》”),根据该等规定,达到一定数量级别的人类基因组数据、个人健康数据等美国人士敏感个人数据将被禁止或限制在美国和中国等受关注国家之间交易。

如,2023年3月2日,BIS以“国家安全”和“外交政策利益”为由,将华大基因旗下的华大生命科学研究院(BGI Research)及香港华大基因科技服务有限公司(BGI Tech Solutions Hongkong)列入实体清单。BIS认为,这两个实体对基因数据的收集和分析构成了极大的风险,可能以此来协助中国政府的监控计划。这使得公司实体许可证将接受多个项目的逐案审查,以及所有其他受EAR约束的项目的拒绝推定。
4. 医疗器械境外准入
在境外准入风险方面,如果医疗器械企业产品出海,目的地国家通常对于医疗器械产品进入当地市场上市及销售存在准入限制。如,在美国的医疗器械准入制度下,依据美国相关法规,美国食品药品监督管理局(Food and Drug Administration,“FDA”)将医疗器械分为三类:低风险的Ⅰ类、中等风险的Ⅱ类和高风险的Ⅲ类。医疗器械产品的制造商和分销商必须进行FDA注册,并根据产品类别提交相应的上市前通知(Premarket Notification,“510(K)”)或上市前批准(Premarket Approval, “PMA”)。对于高风险医疗器械,经销商和分销商还需要通过510(K)认证,提供必要的证明文件,获得FDA批准后才能销售。对于在美国没有办公场所的公司,还必须委任一名FDA注册的美国代理人作为沟通联络人。
如果医疗器械企业的产品出海进行销售,则在目的地国家上市及销售之前,需要获得当地市场的准入许可。数字化转型网www.szhzxw.cn
5. 其他合规
除上述之外,在知识产权、业务运营等领域,医疗器械出海企业也面临着严格的监管。
在知识产权方面,由于部分境外国家可能有更健全的知识产权保护体系,国内的医疗器械企业产品出海面临着更为激烈的知识产权竞争和更为严格的知识产权核查。如自2019年以来,总部位于美国的全球最大的基因测序设备生产商Illumina及子公司在全球范围内对深圳华大智造科技股份有限公司(“华大智造”)发起了一系列的专利、商标侵权诉讼案件,涉及的知识产权(包括专利侵权、商标侵权和不正当竞争)的相关诉讼多达30起。直到2022年7月,华大智造及其关联公司宣布,与Illumina就美国境内的所有未决诉讼达成和解,根据协议条款,双方将不再对美国法院的诉讼判决结果提出异议。至此,华大智造进军美国市场的障碍才扫除。数字化转型网www.szhzxw.cn
在业务运营方面,医疗器械企业出海后,在当地运营需要受到当地的监管。如2024年4月,FDA在官网发布了一则关于医疗器械的安全通讯[17],该通讯涉及对采纳股份全资子公司江苏采纳医疗科技有限公司(“采纳医疗”)出具的进口警示,称其“不符合器械质量体系要求,以防止塑料注射器产品进入美国”。该进口警示将导致采纳医疗部分的医疗器械产品可以被美国海关执行不经检查即扣留,致使部分医用注射器产品暂时无法进入美国市场。
四、结语
医疗器械企业出海已然成为时代趋势和行业热潮,然而在迎接机遇的同时,企业出海无疑也面临着境内和境外目的地国家法律和监管带来多重限制。对此,建议医疗器械企业全面关注出海监管要点,规划设计自身合适的架构及方案,做好出海合规管理工作。
数字化转型网企业出海专题包含哪些内容
数字化转型网企业出海将关注品牌出海,全球化战略,合规与风控,供应链管理,数据保护与隐私安全,知识产权,税务,海外团队建设,海外运营,人力资源管理,组织管理等企业出海、全球化相关全产业链相关环节。数字化转型网www.szhzxw.cn
数字化转型网企业出海专题包含:
1、企业出海、全球化外脑支持:100+企业出海、全球化相关专家、100+企业出海、全球化实践者、1000+相关资料
2、企业出海、全球化研习社:与出海、全球化相关的专家、实践者共同探讨相关问题,推动企业全球化发展! 数字化转型网(www.szhzxw.cn)
3、典型案例参考:与数字化转型网企业出海、全球化研习社社员一起学习典型案例,共探企业全球化发展!

本文由数字化转型网(www.szhzxw.cn)转载而成,来源于网络;编辑/翻译:数字化转型网宁檬树。






