数字化转型网企业出海将关注品牌出海,全球化战略,合规与风控,供应链管理,数据保护与隐私安全,知识产权,税务,海外团队建设,海外运营,人力资源管理,组织管理等企业出海、全球化相关全产业链相关环节。点击图片或扫描图片二维码,加入数字化转型网企业出海研习社:

“出海” 是当下中国生物医药企业扩增收入、提升竞争力和品牌价值的重要发展战略。中国生物医药企业正驶 向国际化 “深海” , 通过海外投资建厂、设立研发机构、技术转让、国际注册认证等多种方式, 全方位参与全 球市场竞争与合作, 整合并优化资源配置, 不断提升自身的国际化创新能力。如何在全球化浪潮中把握确定性, 实现国际化战略宏图, 以寻求新的增量, 是当下中国生物医药行业的一大命题。
一、“出海”是中国医药产业提速扩容的重要手段
1. 中国医药产业概览
中国医药产业蓬勃发展, 药品创新能力显著提升, 市场规模保持增长; 在医疗卫生体系持续升级优 化和国际医药产业格局重塑背景下, “出海” 已成为我国医药企业的重要发展战略
(1)中国医药产业发展概况
我国医药产业发展加速“十三五”期间,生物医药产业已成为国家重点发展的战略性产业。《“十四五”医药工业发展规划》指出,我国规模以上医药工业增加值年均增长9.5%, 高出工业整体增速4.2个百分点; 规模以上企业医药研发投入年均增长约8%, 在研新药数量跃居全球第二位, 超1,000个新药申报临床; 47款国产新药获批上市,278个品种964件通过仿制药质量和疗效一致性评价;出口交货值年均增长14.8%创新药国际注册取得突破性进展, 企业对外投资更加活跃。
“十四五”以来, 我国医药产业面临日益复杂的内、外部环境, 挑战与机遇并存。全球医药产业格局演变, 人人才才技术等医药关键要素国际竞争加剧,产业链、供应链重塑节奏加快, 对我国传统优势出口医药产品提出更高要求, 我国医药产品向价值链更高点的 探索尝试面临挑战 与此同时, 随着药品集采、医保谈判、DRG/DIP支付方式改革、医疗反腐等政策实施深化, 我国医药卫生体制 改革持续推进,医疗保障制度不断完善; 我国经济转向高质量发展, 人民健康消费升级, 对医药产业提出更高要求。”构建以国内 大循环为主体、国内国际双循环相互促进的新发展格局 成为我国医药产业发展的必由之路。‘’
(2)全球医药市场规模分析
海外广阔的医药市场吸引着中国生物医药企业走出国门。据沙利文分析, 全球医药市场规模整体呈现增长趋势,2019年至2023年, 全球医药市场规模从13,245亿美元上升至14,723美元, 预计到2026年、2030年将分别达到17,667亿美元和20,694亿美元 其中, 中国医药市场仅次于美国医药市场, 位居全球第二, 在2023年达到2,315亿美元, 预计到2026年、2030年将分别增长至2,911亿美元、和3,732亿美元。
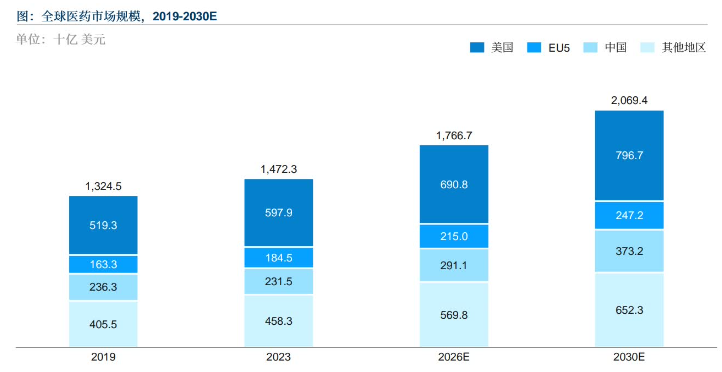
2. 中国医药出海的内在驱动分析——利润承压
随着医保政策改革的不断深化、带量集采的不断扩容, 本土药企面临着产品和利润的双重竞争, 在承压之下出海寻求机遇
(1)医保谈判
为完善我国医疗保障体系, 满足群众对 “好药” 的需求,降低群众医疗负担, 自2017年起我国启用医保谈判制度, 集13亿多参保人用药需求, 通过以量换价” 的市场化机制, 与医药企业进行药品价格磋商, 实现多方共赢。近年来, 每年医保谈判药品数量较为 稳定, 约150个,目录新增药品平均降价幅度维持在60%左右。但由于创新药研发具有投入高、研发周期长、风险高的属性, 医保谈 判带来的降价压力也驱动企业寻求新的增长点。数字化转型网www.szhzxw.cn

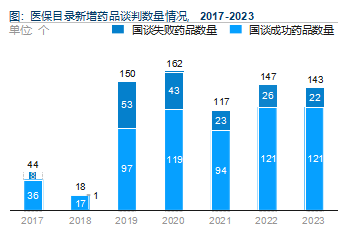
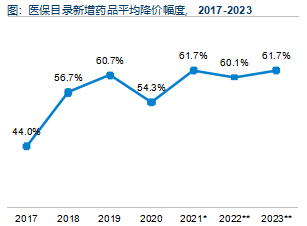
(2)药品集采
药品集中带量采购以来, 平均价格降幅基本保持在50%左右, 近两批集采降价幅度接近60%。国家持续推进药品集采工作, 出台文 件要求扩大集采药品品种和公立医疗机构集采占比。”十四五 全民医疗保障规划提出到2025年, 公立医疗机构通过省级集中采购 平台采购药品金额占全部采购药品 (不含中药饮片) 金额的90%; 国家和各省级 (自治区、直辖市) 药品集中带量采购品种达500个 以上。在药品集采政策下, 医药企业的国内市场利润承压, 驱动企业加快拓展海外市场。
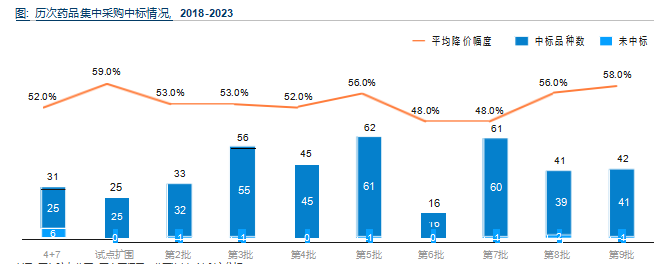
3. 中国医药出海的内在驱动分析——政策利好
我国政府高度重视开展海外贸易, 多项政策多维度支持中国生物医药企业走出国门, 加快融入国际 医药市场全产业链
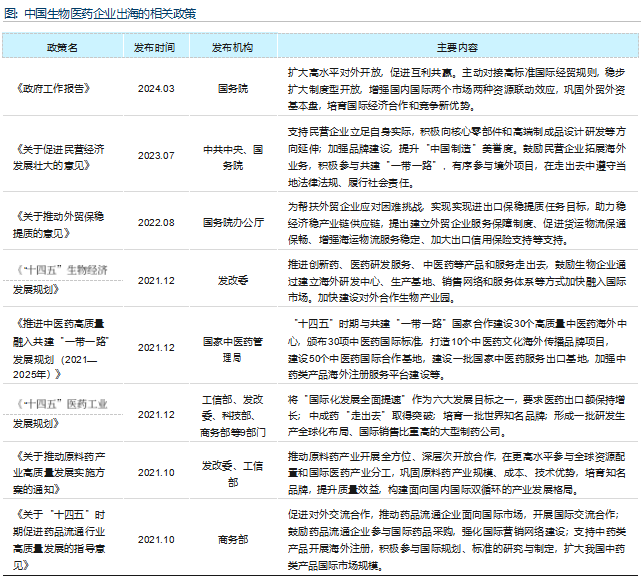
政策鼓励本土医药走向海外
我国政府鼓励医药企业走出国门, 迈向海外市场 2024年的《政府工作报告》提出通过对接国际经贸规则、扩大制度型开放, 扩大《“十四五”生物经济发展规划》、《“十四五”医药工业发展规划》、《关于“十四五”》 时期促进药品流通行业高质量发展的指导意见》等多个十四五规划鼓励中国医药业走出去, 在海外建立研发机构、开展 临床试验、建设生产基地、销售网络、供应链及服务体系, 加快融入国际市场全产业链, 打造国际知名的中国医药品牌 同时, 政策鼓励中国医药企业与 uc一带一路 国家共建境外项目 , 并重视指导企业防范应对贸易保护主义、单边主义等外部挑战, 保障企业 人员在海外的人身和财产安全, 多维度推动我国生物医药出海进程。
4. 中国医药出海的内在驱动分析——创新能力提升
中国医药创新能提快速提升, 在政策支持下, 我国药品临床试验数量增长加快, 创新药获批加速
(1)中国医药研发能力提升, 质量更有保障
近十年, 中国生物医药行业药品研发能力快速提升, 展现出uc中国速度” 。2015年, 国务院发布《关于改革药品医疗器械审评审批 制度的意见》, 针对当时我国药品注册材料质量不高影响审评审批效率, 仿制药与国际先进水平差距大临床急需新药审评时间过长等情况, 要求提高审批审批质量、解决积压申请、加快仿制药一致性评价、鼓励以临床价值为导向的创新药研发等, 推动我国医药创新研发能力提升, 加快 好药新药” 上市。之后, 《关于开展仿制药质量和疗效一致性评价的意见》的印发, 标志国内仿制药质量和疗效一致性评价工作全面展开, 政策推动仿制药研发能力及产业整体提升; 《以临床价值为导向的抗肿瘤药物临床研发指导 原则》出台, 提升了国内肿瘤药临床研发的标准, 为中国临床试验与国际标准的进一步接轨打下基础; 《化学药品注射剂仿制药质量和疗效一致性评价技术要求(征求意见稿) 》发布, 标志注射剂一致性评价正式启动
(2)创新药研发土壤成熟, 创新疗法占比提升
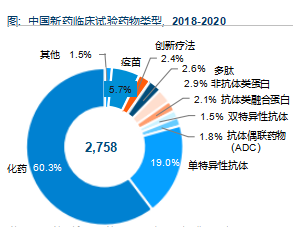
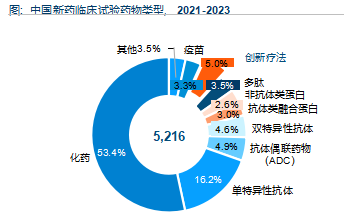
随着中国创新药研发土壤成熟, 近年来, 我国创新药管线数量不断增多.2018-2020年, 我国新药临床试验数量为2,758条, 其中化药占比约60% 抗体类药物研发已有探索。2021-2023年, 我国新药临床试验数量为5,216条, 增长近一倍; 抗体偶联药物(ADC)的临床试验数量占比从1.8%增长至4.9%以基因疗法、溶瘤病毒、核酸药物、细胞治疗为代表的创新疗法占比也在提高。

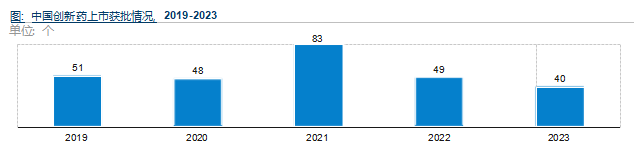
(3)创新药产品获批加速
我国创新药上市获批加速, NMPA发布的2019-2023年的年度药品审评报告显示, 我国创新药获批数量整体处于较高水平。数字化转型网www.szhzxw.cn
5. 中国医药出海的内在驱动分析——接轨国际标准
我国加快与国际医药法规接轨、标准互认和质量互信, 为中国医药产业国际化发展打下坚实的基础, 提升我国药企的国际竞争力
(1)国际人用药品注册技术协调会 (ICH)
ICH是当前全球药品注册领域的核心国际规则制定机制, 其发布的技术指南被全球主要国家药品监管机构接受和转化 2017年6日中国加入ICH 我国药品研发与注册申报开始与国际接轨2019年, 《多区域临床试验计划与设计的一般规则》 (ICH E17指导原则) 落地, 中国药企可实现全球同步研发与注册。《2023年度药品审评报告》指出我国除《Q4B: 药典》和《Q6B: 质量标准: 生物技术产品及生物制品的检查方法及可接受标准》两个指导原则将在2025年版《中国药典》中逐步实施外, 其余ICH指导原则已通过发布 适用公告、接受并翻译指导原则原文的形式实现充分实施O ICH全部指导原则在我国的落地实施工作基本完成,意味着我国药品注册申请、审评审批、质量控制等全面与国际接轨, 中国在药品研发、注册、生产等全生命周期展现出国际化水平
(2)国际药品认证合作组织 (PIS/C)
PIS/C最初是欧盟为保证药品GMP执行的一致性而成立药品检查联盟 (PIC) , 由各国GMP检查机构组成, 后经发展为PIC/S, 成为促进GMP国际交流合作和检查标准统一的重要媒介PIC/S通过制定国际通行的药品GMP指南, 统一各国药品GMP检查标准, 使联 盟成员国药品监管机制之间合作互信加入PIC/S是我国多边GMP互认的需求, 也是未来我国加快推进药品国际化发展的必然选择2021年9月NMPA致函药品检查合作计划(PIC/S) , 申请启动预加入程序随后, 我国积极推进加入PIC/S工作, 加强与PIC/S沟通, 深入研究78个评估指标.2023年9月NMPA正式向PIC/S递交申请材料, 11月 PIC/S致函确认我国为PIC/S正式申请者。未来,我国正式加入PIC/S后, 将促进更新和完善我国GMP标准和相关技术指南, 使我国药品检查体系逐步与国际接轨, 实现药品GMP检 查的国际互认, 提升我国药企的国际竞争力
(3)世界卫生组织预认证 (WHO PQ)
WHO PQ是为帮助发展中国家应对医药监管体系不完善, 对药品的审评及监管能力有限, 但存在公众急需用药的情况而建立的。发展至今,已覆盖免疫接种设备、体外诊断、检验服务、药物(制剂、原料药、药品质控实验室) 、疫苗、病原体传播控制产品等。WHO公布产品评估意向书清单 (Expression of Interest for Product Evaluation) 并负责对申报企业提交的资料进行审评、现场核查、 药品质量及供货稳定性评估, 以确保通过审评的药品安全、有有效效 质量可控。通过WHO PQ认证即成为联合国采购供应商, 产品可在多个发展中国家上市, 显著提高上市效率; 另外, 经过PQ认证的企业, 其生产体系已获得国际权威机构认可, 有助于企业获在全球化中得国际市场的信赖。WHO PQ认证已成为我国疫苗出口的重要途径。截至2024年7月 1 日, WHO官网显示我国已有11款疫苗通过PQ认证, 涉及HPV疫苗、甲肝疫苗、流感疫苗、日本脑炎疫苗、脊灰疫苗、水痘疫苗6大类型
6. 中国医药出海的外在驱动分析
在全球化趋势下, 发达国家市场和 “一带一路” 新兴国家市场是中国医药出口的重点目标
(1)发达国家市场
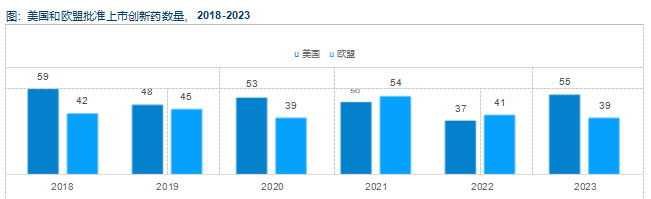
美国、欧洲、日本等发达国家和地区是全球创新药市场的主要集中地, 且持续优先享受创新药品带来的疗效优势与此同时, 发达国家或地区的医疗支付体系通常更为完善。近五年, 美国FDA 以及欧盟EMA批准上市的创新药数量较为稳定, 其中FDA批准的创新 药数量最多, 2018年-2023年累计批准上市302种新分子实体。且创新药的定价水平显著高于中国本土, 我国创新药进军海外市场, 有望开拓更广阔的市场空间, 获得更高的收益水平。数字化转型网www.szhzxw.cn

(2)一带一路” 新兴市场
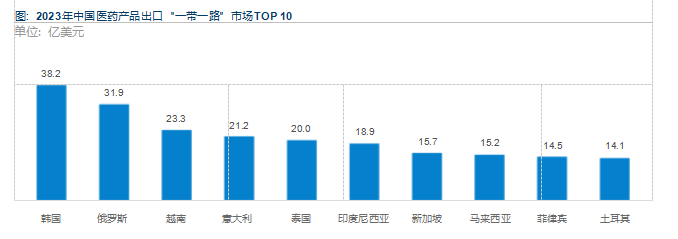
uc一带一路 是我国政府于2013年倡议并主导的跨国经济带, 截至2024年72 , 中国已与154个国家或地区签署了共建 一带一 路” 合作文件, 加入 一带一路 的国家或地区人口数占全球人口总量比例超65%。由于加入一带一路 的国家主要为中、低收 入国家, 其人口基数庞大, 部分国家医疗基础薄弱但卫生支出增长快, 药品自给率较低, 依赖进口, 拥有亟待挖掘市场潜力 中国 医药保健品进出口商会数据显示, 2023年我国在 uc一带一路” 市场中药类和西药类产品出口额分别为18.6亿美元、189.9亿美元, 虽然金额较2022年有所下降, 但仍表现出发展韧性基于一带一路 国家或地区与我国不断升级的自贸协定, 中国医药将加速开辟 新兴市场, 进一步释放国内医药产能
7. 中国医药企业出海策略的战略意图
中国医药企业出海的意图包括提振估值、拓宽销售地域、获取更高收益, 以及提升品牌影响力
(1)提振公司估值 :出海有助于证明公司研发能力和产品竞争力,更重要的证明公司的商业化能力,从而提升公估值
“出海” 不仅是对产品市场价值的有力证明, 更能展现企业在全球范围内的研发实力, 从而增强投资者信心, 提升公司估值2023年12月百利天恒全资子公司Systimmune与百时美施贵宝就BL-B01D1 (EGFR/HER3双特异性抗体药物偶联物) 的开发和商业化权 益达成独家许可与合作协议, 百时美施贵宝将获得BL-B01D1在除中国大陆外的全球其它地区的开发和商业化权益。根据协议, Systimmune将获得8亿美元的首付款, 和最高可达5亿美元的近期或有付款, 开发、注册、销售等里程碑付款最高可获71亿美元额外 付款, 潜在总交易额最高可达84亿美元。该项License-out交易创造了国产药物授权出海交易金额新纪录, 当天百利天恒在科创板的 股价由109.26涨至131.11 单日涨幅20.00%。
(2)拓宽销售地域:广阔的海外市场带来巨大需求,助力本土药企打破国内销售天花板
广阔的国际市场展现出庞大的需求潜力, 助力本土药企打破国内销售天花板, 实现销售和收入的显著增长。汉曲优 (HLX02, 曲妥 珠单抗生物类似药) 是复宏汉霖独立研发的生物制剂。目前, 汉曲优® 已获得包括中国、英国、瑞士、澳大利亚、新加坡、阿根廷、 沙特阿拉伯等近50个国家和地区药品监管机构的上市批准, 商业化权利通过授权协议扩展至全球约100个国家和地区, 显著扩大了其 市场销售范围。销售地域的拓展也有效地提升了汉曲优的全球销售额, 2023年汉曲优®在海外市场的销售额较上一年度实现了 162.3%的增长, 凸显了汉曲优在满足全球患者医疗需求方面的潜力及其出海策略的成功。
(3)获取更高收益:国内内卷激烈,探寻海外新兴市场可进一步释放国内医药产能,获得更大的商业回报
企业实现业绩增长的目标有两条主要路径, 一条是 uc进医保” , 另一条是 “出海” 。随着医保谈判和带量采购政策的深化, 国内医 药行业产品和价格《《双内卷” , 越来越多的国产药企将目光投向海外市场 2023年11月和黄医药研发的呋喹替尼获得FDA批准用 于治疗既往曾接受过相关化疗和靶向治疗的成人转移性结直肠癌患者, 成为首个成功出海的实体瘤TKI抑制剂公开信息显示, 呋喹 替尼5mg*21粒规格产品在美国市场的定价为25,200美元, 约8,456.0元人民币/粒,而在中国市场5mg*7粒的定价为2,513.7元人民币, 约359.1元人民币/粒。呋喹替尼在美国市场定价是中国市场的近24倍。2023年, 上市后一个多月呋喹替尼已实现1,510万美元销售额; 武田财报数据显示, 呋喹替尼从2023年11月上市到2024年Q1结束, 销售额已实现101亿日元, 约6,500万美元, 超过呋喹替尼2023 年H1在中国的销售额5,630万美元。

(4)提升品牌影响力:全球市场对创新能力提出更高要求,企业不断加强自主研发并整合产业链资源,提升品牌价值
随着全球市场对医药创新能力提出更高要求, 企业正不断深化自主研发并整合产业链资源, 以提升品牌价值 百济神州的泽布替尼 是首款全自主临床并自主商业化的国产创新药, 已在65个国家或地区获批, 实现了国产创新药的全球商业化突破 泽布替尼覆盖了包括套细胞淋巴瘤 (MCL)和慢性淋巴细胞白血病 (CLL) /小淋巴细胞淋巴瘤 (SLL) 在内的多种适应症, 并在针对CLL/SLL适应症 的头对头临床试验中展现出比一代BTK抑制剂伊布替尼更优异的疗效和安全性。在25个月随访期内, 疾病进展比例为泽布替尼11% 对比伊布替尼25% 死亡率为泽布替尼3.7%对比伊布替尼5% 客观缓解率(ORR)为泽布替尼93%对比伊布替尼85% 泽布替尼的 无进展生存期 (PFS) 和客观缓解率指标均显著优于伊布替尼,凸显了百济神州的研发能力2023年, 泽布替尼的海外销售额占总销售额的比例高达84.6% 反映了其在全球医药市场的竞争力和在全球医患中的广泛认可。数字化转型网www.szhzxw.cn
二、从原料药海外销售到仿制药出海,再到创新全球化,不断刷新中国医药出海路线图
1. 中国医药出口情况总览
中国医药企业出口总额震荡中有增长, 稳步向高质量发展迈进
(1)中国医药出口概况
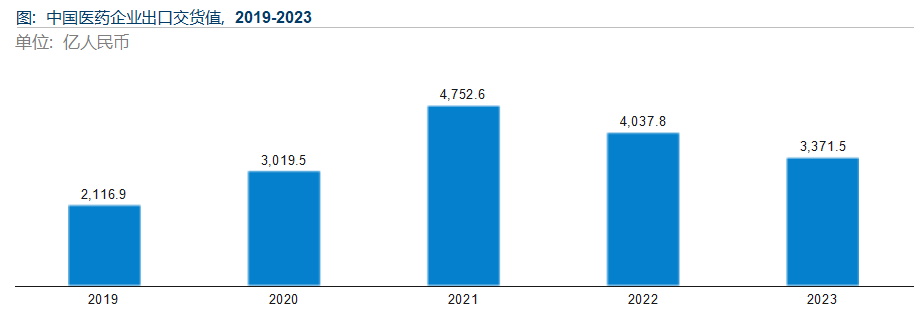
中国医药企业出口总额震荡中有增长, 医药工业稳步向高质量发展迈进, 据中国医药企业管理协会数据显示, 中国医药企业出口交 货值从2019年的2,116.9亿人民币增长至2021年的4,752.6亿人民币, 随后开始回落; 到2023年, 我国医药出口交货值为3,371.5亿人 民币。我国医药出口交货值的下降主要是由于全球新冠疫情得到控制,海外对新冠疫苗等产品的需求量下降。虽然我国出口金额在 2022年开始放缓, 但整体仍保持增长趋势。数字化转型网www.szhzxw.cn
(2)中国医药出口分析
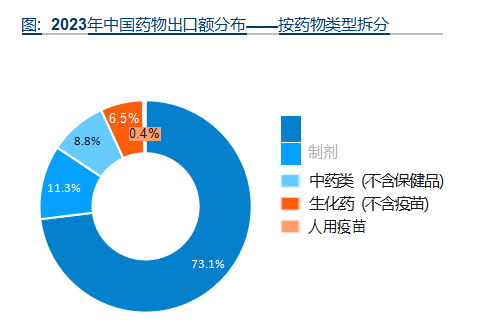
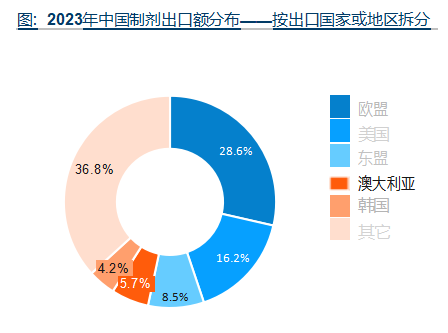
根据中国医药保健品进出口商会数据, 我国2023年出口药物以原料药为主 (73.1%) , 制剂、 中药类 (不含保健品) 、生化药 (除疫苗) 占比分别为11.3% 8.8%和6.5% 按出口国家拆分, 我国制剂主要出口国家或地区为欧盟、 美国、东盟、澳大利亚和韩国, 共占出口额的比例超60%。
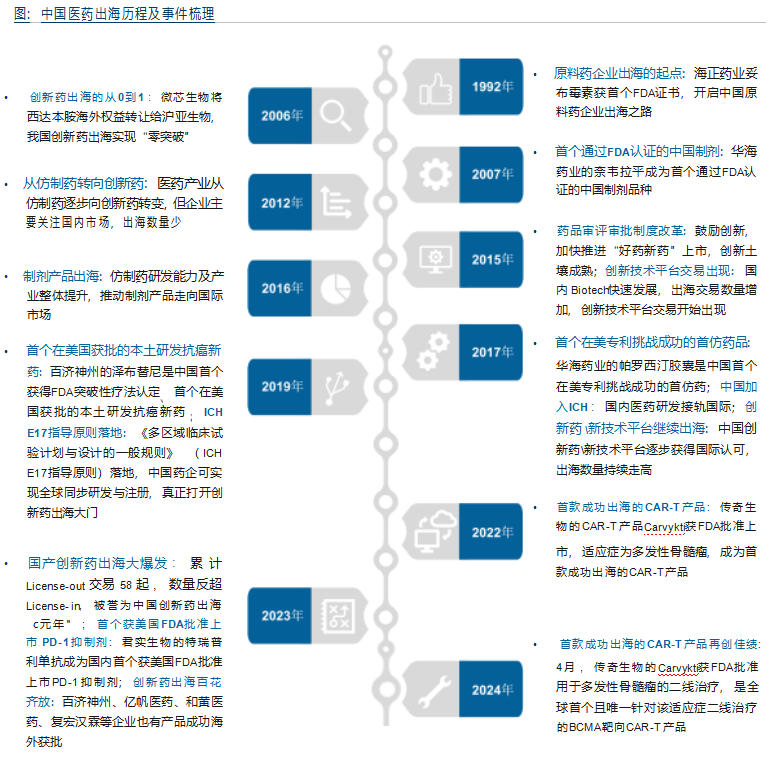
2. 中国医药企业出海历程分析
中国医药出口从原料药到仿制药, 再到创新药, 逐步走向全球医药产业链价值高点
中国医药企业出海历史
1992年, 海正药业获首个FDA证书, 开启中国原料药出海之路; 2006年, 微芯生物转让西达本胺的海外权益, 创新药出海实现了从0到1的突破; 2017年, 华海药业的帕罗西汀胶囊成为首个在美专利挑战成功的首仿药; 2022年, 传奇生物的Carvykti获FDA批准上市, 为首款成功出海的CAR-T产品。从原料药到仿制药再到创新药, 中国医药企业积极应对国际医药市场的激烈竞争。出海已是大势所趋, 未来将有更多的中国医药企业成功出海, 深入融入国际医药全价值链, 让中国医药为更多的患者提供帮助。

三、覆盖发达及新兴国家和地区,中国生物医药持续探索海外市场
1. 发达国家和地区的市场分析——美国
美国医药消费能力强, 人均医疗支出高, 拥有一个多元化且高覆盖率的医疗保障体系;进入美国市 场, 地缘政治因素、支付报销收紧及供应链等挑战应得到重视
(1)宏观经济指标
根据World Bank数据, 2023年美国的国内生产总值 (GDP) 达到27.4万亿美元, GDP增长率为2.5%人均GDP达到8.2万美元, 年增长率为2.0%2023年, 美国总人口达到3.4亿, 人口增长率为0.5%。
医疗支出方面,根据美国医疗保险和医疗补助服务中心数据, 2022年美国医疗支出达到4.5万亿美元,增长4.1%; 人均达到1.4万美元,占当年GDP17.3%。《National Health Expenditure Projections, 2023-32》指出, 预计在未来十年, 美国医疗支出的增长将超过GDP的增长,到2032年医疗保健占GDP的比例将达到19.7% 高于2022年的17.3%。数字化转型网www.szhzxw.cn
(2)医疗保障体系
美国医疗保障系统主要由私人医疗保险 (PHI 、政府医疗保险 (Medicare) 和政府医疗补助 (Medicaid) 组成。其中, Medicare是联邦政府为65岁及以上老年人和某些残障人士提供的健康保险计划; Medicaid是由联邦和州政府共同为收入和资源有限的人士提供, 例如养老院护理、个人护理、医疗服务运输以及家庭和社区服务等; PHI是指由私人健康保险公司销售的健康保险计划, 包括雇主赞助的计划, 且雇主提供的团体医疗保险是美国最主要的保险形式, 2022年覆盖率约65.6%; 另有6%的美国人在工作场所以外的个人/家庭健康保险市场购买私人保险, 包括交易所内和交易所外。
(3)药品监管制度
美国食品与药品管理局(FDA)和州政府卫生局负责美国主管药品监督管理, 其中FDA是药品安全监管主体,包括审评部门(CDER、CBER等)和监管实务办公室(ORA)以及隶属于CDER下的综合质量管理小组 (IQA) 。CDER主要监管处方和非处方药、新药、仿制药上市前评估, 并负责药物的安全性、质量以及有效性工作;CBER负责生物学治疗产品, 保证血液、血液制品、疫苗、过敏原制品以及生物治疗产品的安全性和有效性;ORA检查范围广泛,包括人用和兽用药品、疫苗、医疗器械等。法律方面, 《Federal Food, Drug, and Cosmetic Act (FD&C Act 》是基础法律, 赋予了FDA的监管权并规定了相关审批和监管程序; 《CurrentGood Manufacturing Practice (CGMP)》规定了用于药品生产、加工和包装的方法、设施和控制的最低要求。数字化转型网www.szhzxw.cn
(4)出海美国市场存在的主要挑战
地缘政治因素:2018年以来, 美国政府对我国医疗企业进行了多轮打压, 包括以安全为借口的审查、额外征收关税、对实体和个人实施制裁、制定歧视性法案、限制有关人员流动、推动 供应链脱钩等。
支付报销收紧:鉴于美国老龄化的加重及医疗创新产品增加, 支付方承担的医疗支出持续增长。中国药企应充分了解美国保险公司针对相关药品的报销政策, 掌握主动权, 提升药品的可及性。
供应链本土化:2020年, 美国提出鼓励企业在本土生产药品合原料药, 加快关键原料药战略储备, 以减少对中国等海外供应的过度依赖 未来,中国药企在美国市场将面临床多本土企业的竞争, 跨境产品运输也将面临更严的监管。数字化转型网www.szhzxw.cn

2. 发达国家和地区的市场分析——欧盟
欧盟市场准入管理规范, 医疗支付能力强; 然而欧盟不同国家监管制度存在差异, 出海策略应考量上市国家顺序、 进入方案等。
(1)宏观经济指标
根据World Bank数据, 2023年欧盟27个成员国共有人口4.49亿, 同比增长0.5%; 欧盟GDP为18.4万亿美元, 人均GDP达到4.1万美 元,GDP增长率为0.5%欧盟成员国人口老龄化程度(>65岁)持续加深,欧盟《2024 Aging Reporting》数据分析显示, 2022年欧盟成员国老龄化程度为21%, 意大利、葡萄牙人口老龄化程度最高, 占比均达到了24%预计欧盟成员国老龄化程度将在2070年 增长到30%。2021年,欧盟的医疗总支出为1,591.9十亿欧元,人均医疗卫生支出为3,562欧元,占当年GDP的10.9%。
(2)医疗保障体系
欧盟成员国的医疗保障体系可分为国民公费服务 (NHS) 、社会医疗保险 (SHI 、私人医疗保险 (PHI) 、NHS与SHI结合PHI与 SHI5结合种类型 NHS覆盖全国民众及长期居住者, 按一般税收情况缴纳保险费后可享受统一的医疗福利, 具有普遍、平等、公平 等特点, 代表国家有西班牙、意大利、葡萄牙等; SHI筹资基于医保缴费, 代表国家有法国、奥地利、比利时等; 芬兰采用NHS与SHI结合保障制度;德国采用PHI与SHI结合制度。数字化转型网www.szhzxw.cn
(2)药品监管制度
欧盟药品监管体系由成员国药品监管机构、欧盟委员会和EMA构成。欧盟的药品注册程序包括集中程序 (CP) 、分权程序(DCP)、互认可程序 (MRP) 、成员国程序(INP),欧盟药品局 (EMA)负责CP审批,药品局总部 (HMA) 负责DCP和MRP审批,各成员国药品监管机构负责本国的INP审批。其中,通过CP审批的药品允许上市许可持有人将药品投放整个欧盟市场, 必须采用CP审批的药品包括生物技术衍生产品、孤儿药, 以及活性物质 (2004年5月20 日后获得欧盟授权) 用于治疗艾滋病、癌症、神经退行性疾病或糖尿病的药品, 评估时长为210天。
(4)出海欧盟市场存在的主要挑战
市场环境复杂:欧盟各国在药品注册与医保支付体系上有所不同, 因此, 仅设立单一的市场战略难以 应对各国市场。对于缺乏欧洲市场运营经验的中国公司来说, 满足不同监管机构和支付方的要求是一项较大的挑战。数字化转型网www.szhzxw.cn
进入方案选择:进入欧盟市场的方案可选择成熟的当地企业或MNC合作, 或在欧洲自建运营团队主导或参与产品上市 中国企业应从长远角度出发, 思考并确定公司最终目标是仅在欧洲销售某药品, 迅速回收投资, 还是掌握药品控制权, 在欧洲建立自有品牌。
上市国家顺序:欧盟不同国家之间的准入体系存在差异, 中国药企需考虑国家进入顺序 可选在市场准入相对较易、医保进入相对较快的国家作为首选例如德国, 药品获得EMA批准后可以直接进入德国医保, 且在与医保谈判时, 药企拥有一年的自有定价权。

3. 发达国家和地区的市场分析—— 日本
日本人口老龄化严重, 医疗保障体系完善; 然而,日本监管机构对临床试验要求高、审查严格, 造 成临床研究进展较慢且成本高。
(1)宏观经济指标
根据World Bank数据, 2023年日本人口总数约1.25亿, 同比减少0.5%; 2023年日本GDP达4.21万亿美元, GDP增长率为1.9%, 人均GDP约3.4万美元 根据日本总务省人口统计数据, 2023年日本65岁以上人口达3,624万人,总人口老龄化比例达到了29.0%; 预 计到2070年,每4人中就有1人75岁以上。根据WHO数据, 2021年日本医疗支出达5,417.3亿美元, 占当年GDP 比例为11% 人均医 疗支出达4,347美元。根据Statista数据, 2022年日本人均医疗支出达5,250.6美元,同比增加20.8%。
(2)医疗保障体系
日本的医疗保障属于社会医疗保障模式, 具有强制性,由职工健康保险、居民健康保险、老人健康保险和长期保健保险组成 职工健康保险制度有两个独立的管理系统, 一个是中央政府管理系统, 覆盖中小规模公司的员工; 另一个是保险社团管理系统, 大规模 公司作为独立的保险人 居民健康保险主要针对农业人口、退休人员、自由职业者和无工作人群, 可分为市町村国保和组合国保针对本国人口老龄化持续加重问题,日本建立了老人健康保险和长期保健保险制度 除了强制性健康保险之外, 日本还有营利性的 私人健康保险, 覆盖私立医疗机构的卫生费用并允许使用者付费和共付。医保实现全民覆盖的前提下,日本的卫生筹资全部由公共 医疗保险负担, 价格也受政府统一管理;但卫生服务供给则以《《医疗法人” 等社会资本办医为中心》
(3)药品监管制度
日本的药品安全监管责任由厚生劳动省(MHLW)及药品与医疗器械管理局(PMDA)共同承担MHLW主要由内政部和外设组织组成。医药生活卫生局 (PSEHB) 作为MHLW的内部11个事务局之一,主要确保药品、准药品 (功能性食品、药用化妆品等) 、化妆品、医疗器械等的有效性和安全性, 其中新药的临床试验、审批审查、药品的上市后监督和管理 (再审查、再评价)等职责均在 该局管辖范围之内PMDA主要负责药品从临床研究、注册审查到上市整个过程的科学审查, 上市后安全监测及负责对ADR受害者及药品或生物制品造成的感染者提供补偿性赔偿 日本药品监管领域最高法律《药事法》(PAL) , 后更名为《药品和医疗器械法》 (PMD Act, 简称《药械法》) , 依据此法律,日本制定了一系列政令及省令 (厚生省令) , 共同组成了日本药品法律法规体系。数字化转型网www.szhzxw.cn
(4)出海日本市场存在的主要挑战
临床试验进展慢:日本PMDA法规完善, 对临床试验的要求与细节更严格, 日本民众高度关注临床试验 的风险及副作用, 且因为80%药品可有医保支付, 故愿意参加新药试验的意愿较低, 导致患者入组慢, 临床实验进展缓慢。
先驱审查认定:日本先驱审查制度支持具有全球首创性、处于早期阶段、疗效显著的药物在日本尽快 上市, 是企业进入日本市场的需关注的重要政策 但先驱审查要求将日本作为全球第 一个递交申报的国家, 企业需权衡全球市场战略进行抉择。
MAH营业资质:药品在日本申报上市需具备MAH营业资质,中国企业可选择先在当地建立团队申请 MAH营业资质, 或找当地具有MAH营业资质的代理人申报上市。这对于不熟悉日本市场,没有当地关系网的企业是一大挑战。数字化转型网www.szhzxw.cn

4. 新兴国家和地区的市场分析——东南亚
东南亚市场方兴未艾, 前景宽阔, 但部分国家支付能力有限, 且医药制造基础较薄弱, 监管存在差 异性, 本士化的合作伙伴相对较为稀缺
(1)宏观经济指标
根据World Bank数据, 2023年东南亚地区11个国家总人口数超过6.8亿。东南亚地区总GDP为3.8万亿美金, 但各国经济发展差异显 著, 印尼GDP最高, 为1.4万亿美金, 东帝汶最低, 为22.4亿美金; 人均GDP新加坡最高, 为8.5万美元, 缅甸最低, 为0.1万美元各国经济整体呈现稳步增长, GDP增速最快的国家是菲律宾, 同比增长5.5% 柬埔寨其次, 增长5.4%。
东南亚的医疗保健支出尚未达到全球平均水平, 但预计将迅速增加, 于2030年达到2,700亿美元, 年复合增长率达8%, 其中新加坡 的医疗保健支出将增加200亿美元。此外, 东南亚面临着医疗资源严重短缺的问题, 平均每1,000人口仅0.8名医生。
(2)医疗保障体系
东南亚各国医疗保险制度的总体覆盖率较高, 但医疗水平和医疗资源差距较大。在2021年世界健康安全指数(GHS)榜单中,泰国和新加坡分别位列亚洲第5、第24而柬埔寨和东帝汶分列第126、第154泰国自2001年起实施一项30泰铁计划 的全民医保项目,12岁以上的泰国公民每人每次就医只需自付30泰铁(约合6元人民币) 。新加坡的医疗保障体制包括强制储蓄的《《保健储蓄计划( Medisave) , 个人自愿投保、全国覆盖率超76.5%的《健保双全计划” ( Medishield) 和为贫困人群设立的保健基金计划 (Medifund) 》 。缅甸实行低水平的公费医疗制度,平均每万人仅拥有6.1个医师和6张床位 柬埔寨的医疗保险机制尚未实现全民覆 盖,强制医疗保险仅针对私营部门雇员和公务员。
(3)药品监管制度
东盟国家于1999年成立医药产品工作组 (PPWG) ,希望从区域层面推进东盟各国监管标准协同、监管检查互认,以降低创新药在 各国上市的成本。在ICH、PIC/S等国际标准和原则指导下, 东盟逐步推进各国监管趋同,并成立联合评估协调小组, 试点联合评估程序(JA) ,但目前仅有两个抗疟药通过此程序获批上市。东南亚各个国家药品准入政策不同, 新加坡建立了独立的药品审评审批 监管程序, 其他国家的药品监管体系相对薄弱,主要参考或依赖其他国家的监管决策结果 以药品上市许可(CPP)为例, 新加坡对是否获得其他国家CPP没有要求, 印度尼西亚、马来西亚、菲律宾、泰国等国家则不同程度地要求获得来自其他国家的CPP。
(4)出海东南亚市场存在的主要挑战
合作伙伴有限:东南亚本土药企较少, 虽然市场空间大, 但同时也带了具有相关业务资质的企业少的问题。中国药企在出海东南亚时需谨慎选择合作方, 充分评估拟合作对象的注册能力、 商业化推广能力等。
支付能力较弱:东南亚各国经济水平发展不一, 仅新加坡一个发达国家, 部分国家的医疗支付能力较弱, 这对出海产品的定价及销售策略提出挑战。
监管制度的差异化:东南亚本各国对药品监管的法律、法规与国内存在差异, 不同国家之间也存在不同,如在临床方案设计上, 东南亚各国对标准治疗方案、受试者入组标准等要求不同, 中国在东南亚开展临床研究面临挑战。数字化转型网www.szhzxw.cn

5. 新兴国家和地区的市场分析——巴西
巴西是南美洲主要医药市场, 实行免费医疗制度, 医疗消费随GDP增长而不断提高; 进入巴西市场, 税收和产品注册是两大核心挑战
(1)宏观经济指标
根据World Bank数据, 2023年巴西总人口数达2.2亿,同比增长0.5%; 2023年巴西GDP达2.2万亿美元, GDP增长率为2.9% 人均 GDP约1.0万美元; 2021年巴西医疗支出占GDP 比例为9.9% 人均卫生支出1,625.6美元。根据巴西地理统计研究所 (IBGE) 数据, 巴西人口老龄化问题正在加剧, 2022年巴西≥65岁人口占总人口比例的10.9%,<14岁儿童人口数量占比19.8%。
(2)医疗保障体系
巴西医疗保健系统由公共系统与私营系统组成,提供统一的医疗服务, 而非互补性服务。公共系统具有无偿性与普遍性,私人医疗保险部门具有自愿性。根据IBGE数据,除医疗诊断和治疗, 公共系统还为部分慢性疾病提供免费药物, 并针对老人和儿童提供国家疫苗接种计划。作为巴西公共医疗体系的一部分, 统一医疗保健系统 (SUS) 是大约72%人口的医疗服务唯一提供者,而私人健康保险公司运营的私立保险则为有支付能力的群体提供服务巴西公共医疗保健系统参与度和医疗支出比例水平较低, 公共医疗保健系统以100%人口覆盖率却仅占医疗保健总支出的41% 而私营部门以25%的人口覆盖率承担了59%的医疗保健总支出占比。
(3)药品监管制度
巴西的药品监管制度主要由巴西国家卫生监督局 (ANVISA) 负责。ANVISA的主要职责是通过执行对生产、营销和使用受卫生法规约束的药品、医疗器械等产品和服务的卫生控制,促进公众健康的保护OANVISA还负责对相关的环境、工艺、成分和技术进行监管, 并在港口、机场和边境实施控制,以确保卫生标准的严格执行 药品由ANVISA负责全面监管, 包括临床试验许可、API及药品和生 物制品的市场授权,以及上市后变更管理。药品监管类别包含新合成和半合成药物、仿制药、类似药物(品牌仿制药) 、强效药(顺势疗法、哲学药物和抗同毒药) 、特定药物、通知药物(低风险) 、OTC药物、草药药物、医用气体、生物制品和放射性药物。其中新合成和半合成药物、仿制药、类似药物 (品牌仿制药) 分别主要依据法规RDC 753/2023、RDC 753/2023、RDC 753/2023; 临床试验的提交和批准依据包括RDC09/2015和RDC205/2017(罕见病特别程序) 。数字化转型网www.szhzxw.cn
(4)出海巴西市场存在的主要挑战
税收挑战:巴西的税收制度是全球最复杂的税收制度之一, 不同州、市、联邦有各自的税种及税 率。这意味着中国企业进入巴西市场时, 需要充分了解每个细分市场的税收政策, 做 好税收筹划, 可通过专业税务咨询机构帮助制定税收策略。
产品注册:巴西药品审查制度严格, 在南美地区是先行制定生物药品标准的国家之一 巴西政府 只接受巴西国内生产商或国内进口商对健康产品进行注册。同时, 申请注册企业还需 持有AFE资质, 境外制造商不能更换AFEo 因而进入巴西市场, 在税务咨询以及产品 注册过程中, 企业可以寻求专业的合作伙伴。

6. 新兴国家和地区的市场分析——中东
中东地区国家经济水平差异大, 医疗保障及监管制度不一;进入中东市场, 面临着医疗需求差异、 政治动荡、 监管差异及绿色发展等挑战
(1)宏观经济指标
根据World Bank数据, 2023年中东与北非地区人口总数约5.0亿, 同比增长1.5%; GDP达4.3万亿美元, 人均约8,561.9美元。其中, 埃及人口最多, 2023年口总数达1.1亿, 伊朗位列第二, 总人口数约8,917.28万人。GDP排名第一的国家是沙特阿拉伯, 2023年达 3,959.3亿美元, GDP增长率达3.8% 人均约3,512.6美元; 卡塔尔是中东地区人均GDP最高的国家, 高达8.75万美元2021年黎巴 嫩医疗支出占GDP 比例10.1% 位列第一; 阿联酋国内人均私人医疗支出最多, 2021年约1,459.3美元。商务部预测到2025年沙特医 疗保健支出总额将达到2,200亿里亚尔。数字化转型网www.szhzxw.cn
(2)医疗保障体系
沙特阿拉伯的医疗保健系统由公立和私立医疗服务体系组成 目前主要通过卫生部并通过其他政府卫生机构加强向所有沙特公民和在公共部门工作的外籍人士免费提供医疗保健,私营部门在提供医疗保健服务方面的作用和参与也不断增加, 政府要求在私营部门工作的外籍人士享有由雇主支付的一定程度的医疗保险阿联酋要求所有公民和居民参加健康保险体系, 所有雇主必须为雇员及其家属提供健康保险,自2025年起私营部门雇员和家庭佣工将被纳入强制医疗保险计划, 规定要求私营部门为雇员购买强制医疗保险。
(3)药品监管制度
阿布扎比卫生署(DOH)是阿联酋首都阿布扎比酋长国医疗保健部门的监管机构, 2023年成立的阿联酋药品管理局(EDE)将取代原阿联酋卫生预防部 (MOHAP)接管药品和医疗器械的监管工作, 药品监管主要依照《药品和药用产品法》。约旦食品药品管理局(JFDA)是约旦唯一负责药品安全与有效性的公共部门监管机构, 主要依据有《药品和药剂法》、《药学研究法》、《公共卫生法》和《食品和药品总组织法》等。
(4)出海中东市场存在的主要挑战
政治局势的动荡:中东地区存在宗教、政治、民族等矛盾问题, 地区秩序呈现碎片化, 部分国家安全形势严峻。政治局势的复杂多变, 可能对供应链稳定性造成影响。中国药企需要建立稳定的供应链体系, 确保产品的及时供应和质量安全。
严格的监管制度:中国药企需要深入了解并遵守当地的法律法规, 确保产品的合规性。例如, 沙特的 《企业及药品和草药制剂条例》要求从事药品和草药制剂贸易的工厂及仓库必须有足够所有注册制剂保存6个月的永久库存, 若预期注册制剂供应中断或短缺,则涉嫌违 规, 将被处以罚金。
绿色发展高要求:部分中东地区国家重视零碳绿色发展, 对于ESG相关要求越来越高, 这提高了在当地 建厂及运营的成本。数字化转型网www.szhzxw.cn
数字化转型网企业出海专题包含哪些内容
数字化转型网企业出海将关注品牌出海,全球化战略,合规与风控,供应链管理,数据保护与隐私安全,知识产权,税务,海外团队建设,海外运营,人力资源管理,组织管理等企业出海、全球化相关全产业链相关环节。数字化转型网www.szhzxw.cn
数字化转型网企业出海专题包含:
1、企业出海、全球化外脑支持:100+企业出海、全球化相关专家、100+企业出海、全球化实践者、1000+相关资料
2、企业出海、全球化研习社:与出海、全球化相关的专家、实践者共同探讨相关问题,推动企业全球化发展! 数字化转型网(www.szhzxw.cn)
3、典型案例参考:与数字化转型网企业出海、全球化研习社社员一起学习典型案例,共探企业全球化发展!

本文由数字化转型网(www.szhzxw.cn)转载而成,来源于药械出海百晓生;编辑/翻译:数字化转型网宁檬树。





