数据专题将关注数据治理、数据质量管理、数据架构、主数据管理、数据仓库、元数据管理、数据备份、数据挖掘、数据分析、数据安全、大数据、数据合规、等数据相关全产业链相关环节。
当今的制药行业,严格遵守良好生产规范 (GMP) 对于确保产品安全、质量和一致性至关重要。实现 GMP 合规性的关键要素在于有效管理数据,特别是 GMP 流程中的主数据。从生产工作流程到质量控制,强大的数据管理构成了高效合规的制药制造环境的基础。
本文探讨了主数据在 GMP 中的重要作用,并深入了解了它如何影响制造流程和质量控制。
一、GMP 中主数据的基本要素
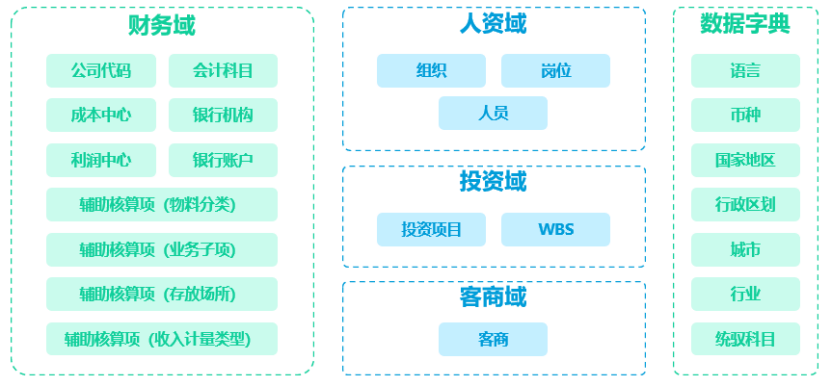
主数据是 GMP 流程的基础,可确保所有操作的一致性。它包括有关药品制造中使用的材料、设备、工艺和人员的关键信息。每个部门都依赖准确的数据来确保无缝的工作流程。如果没有精确的主数据,错误可能会扰乱生产并导致合规风险。因此,公司需要维护可靠的数据以满足监管要求并确保产品质量。主数据确保可追溯性,帮助团队从头到尾跟踪材料和流程。它还通过为监管机构提供透明的文档来支持审计。
此外,主数据可实现部门之间的顺畅沟通。当所有团队使用相同的数据时,误解就会减少。生产、质量控制和供应链团队可以更有效地协调他们的工作。这种协调减少了延迟,确保流程高效运行并符合 GMP 标准。此外,及时更新主数据可防止过时的信息影响运营。一致的数据管理还通过提供实时洞察来支持决策。总体而言,在 GMP 中使用主数据可确保更好的运营控制、更少的错误和更高的产品安全性。
二、GMP 中主数据的关键组成部分
主数据包含支持 GMP 活动的几个关键组件。每个组件在维持整个生产周期的一致性和合规性方面都发挥着至关重要的作用:
材料数据:有关原材料的准确信息,包括来源、规格和质量属性。
设备数据:机械和设备的综合记录,包括校准计划和性能历史记录。
过程数据:制造过程的标准化描述,包括操作程序和关键参数。
人事资料:参与 GMP 流程的人员的培训、认证和职责记录。
供应商数据:有关核准供应商及其资质和业绩历史的信息。
产品数据:生产的每种产品的规格、配方和批次记录。
三、主数据对制造效率的影响
简化生产工作流程
主数据通过保持基本信息的有序性和可访问性来确保生产工作流程顺利运行。GMP 中的准确数据可最大限度地减少生产错误,帮助团队保持正常运转而不会中断。当原材料、设备和流程与更新的数据保持一致时,运营将变得更加高效。团队可以轻松避免因材料规格不正确或设备详细信息缺失而导致的延误。这种一致性可提高生产力并使生产保持最佳速度。
此外,管理良好的主数据可帮助制造商减少浪费并防止停机。有了可靠的数据,团队便可在潜在问题影响生产之前快速识别它们。协调的工作流程还可改善跨部门协作,确保每个流程同步运行。及时更新主数据可帮助生产团队更快地应对意外变化。因此,公司可实现更顺畅的运营、更好的产品质量和更少的代价高昂的中断。
加强批次记录管理
在 GMP 制造中,维护详细而准确的批次记录可确保合规性和产品可追溯性。这些记录记录了从原材料到成品的每个生产步骤。凭借精确的批次记录,公司可以满足监管标准并确保产品质量。主数据通过为每个批次提供一致的参考点来支持这些记录。因此,生产团队可以毫不费力地跟踪材料、设备和流程。这种一致性增强了可追溯性,并在出现问题时可以更快地进行故障排除。
将 GMP 中的数据集成到批次记录系统中可改善监督并简化合规工作。借助集中数据,公司可以快速识别生产过程中的偏差。这种可见性有助于团队进行彻底调查并及时实施纠正措施。清晰的批次记录还可以通过让监管机构透明地访问生产数据来简化审计。
四、在 GMP 制造中利用主数据的优势
提高数据准确性:集中的主数据确保所有部门都使用一致且准确的信息。
增强监管合规性:GMP 中的准确数据有助于满足严格的监管要求,降低不合规风险。
提高可追溯性:主数据提供了清晰的审计跟踪,便于在出现偏差或质量问题时进行调查。
减少人为错误:跨部门的标准化数据最大限度地减少了因手动输入数据而导致错误的可能性。
优化库存管理:准确的材料和供应商数据简化了库存控制,降低了缺货或生产过剩的风险。
五、GMP 主数据管理面临的挑战
数据集成:制药公司在管理主数据时面临的主要挑战之一是将其集成到多个系统中。通常,数据分散在不同的部门或软件平台中,很难确保一致性。解决此问题需要实施集成软件解决方案,将 GMP 中的数据集中化并确保所有团队使用相同的信息。
持数据准确性:长期保持主数据的准确性是另一项重大挑战。随着材料、设备和工艺的发展,公司必须确保定期更新主数据。不这样做可能会导致影响合规性和生产效率的差异。定期审计和强大的数据治理政策对于克服这一挑战至关重要。
确保数据安全:在 GMP 环境中,保护主数据免受未经授权的访问是另一个挑战。制药公司处理的敏感数据必须保持安全,同时还要遵守法规要求。任何数据泄露或未经授权的更改都可能损害产品质量并危及合规性。为了降低这种风险,公司必须建立严格的访问控制并实施加密协议。定期的安全审核也有助于识别漏洞并确保系统安全。
六、主数据在质量控制中的作用
确保质量测试的一致性
主数据可确保质量控制流程在每个批次和生产运行中保持一致。它为材料、设备和工艺提供 GMP 中的标准化数据,确保所有测试都遵循预定义的规范。当数据保持一致时,质量控制团队可以执行可靠的测试而不会产生混淆或延迟。这种一致性减少了批次之间的差异,帮助公司保持统一的产品质量。因此,一致的数据管理可提高合规性并在审计期间支持更好的结果。
此外,主数据可帮助团队在质量测试期间快速识别差异。有了准确的参考点,质量控制可以在偏差影响产品安全之前发现偏差。这种主动方法可以加强整体质量管理体系并最大限度地降低风险。此外,同步数据可以改善生产和质量控制之间的协作,确保无缝的工作流程。定期更新主数据可使测试与不断发展的标准保持一致,确保公司满足监管要求。最终,使用一致的数据可以提高产品安全性并增强监管机构和客户的信任。
支持纠正和预防措施
准确的主数据可帮助团队在出现质量问题时迅速采取行动。它提供 GMP 中的一致数据,使识别偏差的根本原因变得更加容易。有了可靠的数据,团队可以实施直接解决问题的纠正措施。这种精确度可减少停机时间并确保产品符合监管标准。此外,快速访问准确的数据使团队能够在问题升级之前采取行动,从而提高整体效率。
主数据还可以通过使操作与更新的信息保持一致来加强预防措施。团队可以在实施 CAPA 解决方案后更新数据,防止将来再次发生类似问题。这种持续改进可确保流程始终符合 GMP 要求。此外,使用主数据可以增强 CAPA 调查期间部门之间的沟通,促进更好的协作。当数据保持最新时,团队可以预测潜在风险并主动解决它们。最终,将 CAPA 与主数据管理集成可确保更顺畅的运营和一致的产品质量。
七、GMP 中管理主数据的最佳实践
实施数据治理政策
为所有部门的数据所有权、管理和维护制定明确的指导方针。
定期数据审核
定期审查主数据以确保准确性、一致性和完整性。
自动化数据输入流程
使用自动化系统捕获和更新主数据,降低人为错误的风险。
跨部门协作
鼓励生产、质量控制和监管团队之间的协作,以确保主数据标准的一致性。
每次更改后更新数据
确保主数据在材料、工艺或设备发生变化后及时更新,以保持符合 GMP 标准。
八、结论
主数据管理是药品制造和质量控制中 GMP 合规性的关键组成部分。通过确保 GMP 中的数据保持准确、一致且可在所有部门访问,公司可以简化生产流程、加强质量控制并保持法规遵从性。实施主数据管理的最佳实践(例如数据治理政策和定期审计)将有助于制药公司提高效率并降低不合规风险。最终,主数据在 GMP 制造中的作用是基础性的,支持从生产工作流程到法规遵从性的一切。
声明:本文来自网络,版权归作者所有。文章内容仅代表作者独立观点,不代表数字化转型网立场,转载目的在于传递更多信息。如有侵权,请联系我们。数字化转型网www.szhzxw.cn
数字化转型网数据专题包含哪些内容
数字化转型网数据专题将关注数据治理、数据质量管理、数据架构、主数据管理、数据仓库、元数据管理、数据备份、数据挖掘、数据分析、数据安全、大数据、数据合规、等数据相关全产业链相关环节。
数字化转型网数据专题包含: 数字化转型网(www.szhzxw.cn)
1、数据相关外脑支持:100+数据相关专家、100+数据实践者、1000+相关资料
2、数据研习社:与全球数据相关专家、实践者共同探讨相关问题,推动产业发展!
3、国际认证培训:目前已引进DAMA国际认证CDMP,其他国内外认证也在逐步引进中
4、典型案例参考:与数字化转型网数据要素X研习社社员一起学习典型案例,共探企业数据落地应用
本文由数字化转型网(www.szhzxw.cn)转载而成,来源于网络;编辑/翻译:数字化转型网默然。